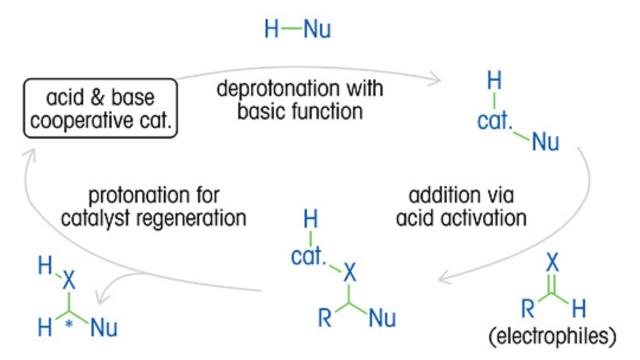
Глубокое понимание кинетики реакции, механизма, каталитических циклов и влияния переменных имеет важное значение для оптимизации энантиомерных соотношений и выхода продукта, а также для снижения затрат и отходов.
Для получения точных данных решающее значение имеет точный контроль основных параметров реакции, таких как температура, давление, скорость дозирования реагента и скорость перемешивания. Автоматизированные лабораторные реакторы широко используются в академических и промышленных учреждениях для достижения такого контроля. Недавнее расширение возможностей лабораторных реакторов EasyMax™ за счет точного контроля температуры до -78 °C расширяет пространство для проектирования каталитических процессов.
Превосходное управление реактором повышает точность измерений реакций, включая анализ реагентов, реагентов, форм катализаторов, переходных промежуточных продуктов и примесей побочных продуктов. Отслеживание реакционных веществ в режиме реального времени позволяет собирать обширные данные эксперименты, которые могут помочь в разработке кинетических параметров и поддержать предполагаемые механизмы реакций, включая каталитические циклы.
ИК-Фурье спектроскопия in situ, ИК-Фурье спектроскопия в реальном времени и рамановская спектроскопия являются признанными методами для более глубокого понимания каталитических реакций. Спектрометры ReactIR™ и ReactRaman™ были разработаны для анализа химических реакций, предлагая ряд вставных зондов и проточных ячеек, которые могут работать в широком диапазоне температур и давлений, часто необходимых для исследований каталитических реакций.
Автоматизированный отбор проб химических реакций позволяет повысить производительность за счет решения задач в двух масштабах:
- Инструменты для ручного отбора проб, такие как пипетки и шприцы
- Сам процесс ручного отбора проб со сложными реакциями, чувствительными к температуре, давлению или воздуху
EasySampler™ — это автоматизированная система отбора проб в реакторе, предназначенная для поточного сбора, тушения и разбавления реакционных образцов. Это позволяет извлекать пробы в условиях реакции и устраняет проблемы, связанные с ручным отбором проб.
DirectInject-LC™ обеспечивает анализ химических реакций в режиме реального времени на месте с использованием хроматографических измерений. Автоматизированная система решает сложные проблемы, связанные с хроматографией, такие как отбор проб реакции, гашение, разбавление и взаимодействие с хроматографом. DirectInject-LC дифференцирует и измеряет ключевые вещества по мере протекания реакции, обеспечивая глубокое понимание кинетики реакции, механизма и влияния переменных на исход реакции. DirectInject-LC взаимодействует с системами ВЭЖХ-МС, ВЭЖХ и хиральными системами ВЭЖХ для расширенных возможностей разделения и анализа.
При масштабировании каталитических реакций последние достижения в области моделирования химических реакций предоставляют информацию, необходимую для более безопасных реакций с большим выходом и меньшим количеством примесей. Динамическое моделирование экспериментальных данных также позволяет глубже понять кинетику реакции и влияние переменных реакции.