ما هي معالجة المصب الصيدلانية الحيوية (DSP)؟
المعالجة النهائية (DSP) هي سلسلة من عمليات الوحدة بعد الانتهاء من نمو الخلايا وتوسعها ، والإنتاج أو التخليق المكتمل للمواد الدوائية أو المكونات الأخرى. تهدف المعالجة النهائية إلى عزل وتنقية وتركيز مادة الدواء (DS) التي تم تصنيعها مسبقا أو أي منتج آخر من مصفوفة النمو بالجملة. تاريخيا ، تم الاستثمار لتحسين الغلة والعيار في المنبع ، مما يجعل تطوير الأدوية البيولوجية أكثر اقتصادا. في السنوات السابقة ، لم تتم معالجة العمليات النهائية على نفس المستوى وتتطلب الآن مزيدا من التحسين.
تشير المعالجة النهائية للمستحضرات الصيدلانية الحيوية إلى استعادة وتنقية مادة دوائية من مصادر طبيعية ، مثل الخلايا الحيوانية أو البكتيرية. ينطبق DSP الصيدلانية الحيوية في الأجسام المضادة وحيدة النسيلة (mAb) أو عمليات البروتين وتصنيع قليل النوكليوتيدات والسكريات واللقاحات المختلفة والاقتران الحيوي والعلاجات الجينية ومنتجات العلاج الخلوي.
قد تشمل المعالجة النهائية أنشطة الصياغة الأولية ، مما يدل على الانتقال من DS إلى منتج دوائي (DP). تشمل الاعتبارات المهمة إدارة وقياس سمات جودة المنتج ، ومعلمات العملية المتعددة ، ومصادر وكميات الشوائب ، وتيارات النفايات ، والمخاطر البيولوجية.
يتم تنفيذ أنشطة DSP على نطاق تطوير العمليات على نطاق المختبر ، والمقاييس التجريبية ، والتصنيع وبمساعدة فرق التكنولوجيا التحليلية للعملية (PAT) وعلوم وتكنولوجيا التصنيع (MSAT) التي تركز على تحسين العملية وتوسيع نطاقها واستكشاف الأخطاء وإصلاحها. المعالجة النهائية المماثلة في مقاييس بيولوجيا الاكتشاف أو المراحل المبكرة من فحص الهدف عالي الإنتاجية ليست شائعة ، على الرغم من أنه يمكن إجراؤها بالمثل ، من حيث المبدأ.
6 تقنيات مبتكرة للمعالجة الحيوية النهائية
يناقش هذا الدليل كيفية استخدام العلماء للتكنولوجيا التحليلية للعمليات (PAT) لتحويل سير العمل اليومي وتحسين العمليات النهائية بشكل كبير. تشمل المواضيع:
- مراقبة تركيز البروتين
- تحسين عملية تبادل المخزن المؤقت
- تكوين اللقاح المساعد وتوزيعه ومورفولوجيته
- أتمتة تعطيل الفيروس
- تطوير عملية الاقتران الحيوي
ما هي الخطوات والأدوات المرتبطة بالمعالجة النهائية
1. الحصاد: المعالجات المسبقة ، الطرد المركزي ، والترشيح
- ما قبل العلاج:
تحلل الفاعل بالسطح ، امتصاص المرحلة العضوية: عادة ما يسعى فصل المنتج مع التحلل إلى تحقيق هدف أساسي: تعطيل هياكل العزل التي تحتوي على مادة أو منتج الدواء بشكل فعال وخلق فصل مادي بين أي حطام وشوائب ومادة الدواء. يتم استخدام تحلل الحمض أو الفاعل بالسطح بشكل حصري تقريبا مع المزارع البكتيرية أو الخميرة. وبالمثل ، فإن امتصاص الطور العضوي والتقاط المنتج هو الأكثر شيوعا بين أنظمة التعبير والإنتاج البكتيرية ويستخدم أحيانا لأنظمة الخميرة.
التلبد وهطول الأمطار: هذه طرق للتلاعب بنظام الجسيمات النشط لتحقيق هدف الفصل. يتم تطبيق التلبد بشكل عام كطريقة للتحضير قبل الترشيح أو الطرد المركزي. يضمن تطبيق التلبد تدفقا عاليا للكتلة على وحدات الترشيح بالإضافة إلى الفصل الفعال والفعال من حيث التكلفة لمادة الخلية عن المادة الطافية. قد تكون هناك حاجة إلى طرق إضافية لإزالة الندف وبروتوكولات التحقق. الترسيب هو معالجة نشطة للجسيمات ناتجة عن تغيير المعلمات ، مثل المذيب والقوة الأيونية لتقليل الذوبان. - الطرد المركزي: تم اعتماد الطرد المركزي على نطاق واسع كطريقة للفصل في المعالجة الحيوية ، وهو تقنية شائعة ورئيسية تستخدم لفصل حطام الجسيمات بشكل عشوائي بناء على الكتلة أو الوزن الجزيئي كدالة لسرعة الوعاء ومعدلات التعبئة والتفريغ. تزيل أجهزة الطرد المركزي الصناعية الشائعة كميات كبيرة (تصل إلى 99٪) من كتلة الجسيمات لأحجام الجسيمات الصغيرة التي تصل إلى 5 ميكرومتر ، وأحيانا صغيرة تصل إلى 1 ميكرومتر للعمليات المحسنة للغاية. على الرغم من هذه الكفاءة ، لا يزال بإمكان أجهزة الطرد المركزي تمرير كميات إشكالية من الجسيمات الدقيقة ، وخاصة الجسيمات النانوية ، إلى عمليات المصب التي تتطلب مزيدا من المعالجة. مع العمليات الحيوية التي تحقق عادة كتلة حيوية إجمالية عالية إلى عالية جدا (الجسيمات الدقيقة والنانوية) وكثافات الخلايا النهائية القابلة للحياة المتغيرة ، يمكن لقدرات الطرد المركزي الثابتة أيضا أن تحد من إنتاجية العملية ولا تعتبر عملية على نطاق واسع للمعالجة الحيوية المستمرة.
- ترشيح العمق ، الألياف المجوفة: اعتمادا على طبيعة المنتج والعملية ، تتضمن طرق الحصاد عادة ترشيح العمق (الشكل 1-1) أو مرشحات الألياف المجوفة (الشكل 1-2). مع الترشيح العميق ، يتم ضخ خليط يحتوي على جزيئات من خلال غشاء أو واجهة أخرى لفصل الحطام عن المنتج في تعليق سائل. تستخدم مرشحات الألياف المجوفة في عمليات المعالجة الحيوية المستمرة لإزالة مادة الدواء المعبر عنها بالمادة الطافية (DS) مع حبس جزء من الكتلة الحيوية مؤقتا في الألياف المجوفة قبل التدفق العكسي باستخدام وسائط التدفق المعاكس. ويعد فصل تدفق المجال الصوتي تقنية ناشئة أخرى توجد حاليا في الغالب في بيئات التنمية. مع أوضاع التشغيل والتكوين المختلفة، يمكن للنتائج:
- عدم تعديل أي فصل للخلايا أو الجسيمات (الشكل 1-3 أ)
- حدد فصل الخلية أو الجسيمات من تدفقات التغذية في دفق التقاط جديد مع تحويل أو فصل مجموعة جسيمات ثانية (الشكل 1-3 ب)
- نقل نظام جسيمات كامل إلى تيار جديد و / أو إعادة تخصيص السوائل ، ربما في إعادة التدوير (الشكل 1 - 3 ج)
- تتفاعل هيدروديناميكيا ، حيث قد يحدث خليط معدل لكل من اختيار الجسيمات وتبادل السوائل (الشكل 1-3 د)

من المعروف أن توزيع حجم الجسيمات (PSD) هو معلمة عملية حرجة (CPP) تشارك في سعة المرشح وهي أكثر تأثيرا من التعكر والضغط وحدهما. يمكن دمج PSD بمرور الوقت لتعيين تراكم الجسيمات على المرشحات (المسبار فوق المرشح) والتنبؤ بالفشل. يمكن أيضا قياس PSD أسفل المرشح لمراقبة اختراقات الجسيمات النزيلة وتحديد الأحداث المماثلة.
تقيس أجهزة تحليل حجم الجسيمات المضمنة ، مثل ParticleTrack™ بتقنية FBRM® ، تراكم الجسيمات وتوزيع حجم تغذية مرق الخلية التي تدخل المرشحات أو الهروب منها ويمكن أن توفر ارتباط السعة أو التحكم في التغذية الراجعة لتقليل اضطرابات العملية. يقوم EasyViewer™ مع Image2Chords™ بإجراء تحليل للصور واستخراج تراكم الجسيمات وتوزيع الحجم والتشكل من الصور المضمنة التي تم حلها بمرور الوقت للعملية. يمكن أن يوفر EasyViewer ، الذي يتم وضعه أعلى أو أسفل المرشحات ، ارتباط السعة أو التحكم في التغذية الراجعة ولكنه يكون أكثر قيمة عند تطبيقه لتحليل السبب الجذري والتوصيف والتشكل.

2. التقاط
تتغير طريقة واستراتيجية الالتقاط قليلا اعتمادا على طبيعة الجزيء المستهدف. يتم التقاط الأجسام المضادة بواسطة راتنجات التقارب مثل البروتين A والبروتين G ، بالإضافة إلى بعض الطرق الأخرى المصممة بشكل انتقائي. غالبا ما يتم التقاط البروتينات غير الأجسام المضادة وقليل النوكليوتيدات بواسطة كروماتوغرافيا التبادل الأيوني (IEX). غالبا ما يتم التقاط منتجات مثل السكريات وهياكل الجليكان المعقدة عن طريق كروماتوغرافيا التفاعل الكارهة للماء (HIC) أو كروماتوغرافيا الطور العكسي (RPC).
تتضمن أهداف القياس الرئيسية أثناء الكروماتوغرافيا تعظيم سعة ربط المنتج بالعمود ، والتي تقاس بكتلة المنتج المحمل على العمود (حمل العمود) ، مطروحا منها كتلة المنتج الذي يهرب من مخرج العمود (المعروف باسم "الاختراق"). الأشعة فوق البنفسجية هي الطريقة الأكثر شيوعا لقياس المنتج ، وتستخدم على نطاق واسع لقياس البروتين والحمض النووي. من الممكن أيضا استخدام طرق بديلة لقياسات المنتج وغير المنتج. يمكن استخدام التحليل الطيفي FTIR المضمن للقياس الكمي والتمييز بين المكونات مثل المواد الخافضة للتوتر السطحي ، ومخازن السكر أو الأحماض الأمينية الشائعة ، والدهون ، والمنتجات المترافقة ، وحتى المنتجات ذات الهياكل المتغيرة ، مثل تلك الخاصة بالشظايا أو المونومر أو الأشكال المجمعة من mAbs. غالبا ما يستخدم FTIR بالإضافة إلى الأشعة فوق البنفسجية عندما تكون الأشعة فوق البنفسجية وحدها غير قادرة على قياس المكونات المهمة غير البروتينية / الحمض النووي.
- كروماتوغرافيا التقارب (بروتين A / G) هي طريقة كروماتوغرافية من التمرير الأول (تسمى عادة البروتين A أو ProA) التي تفصل وتركز المنتج محل الاهتمام (عادة ما يكون مللي أمبير) عن المواد الأخرى القابلة للذوبان عن طريق ربط البروتين المستهدف أو الاحتفاظ به بشكل عكسي بالعمود عبر تفاعلات ربط محددة (الصورة أ) بينما المكونات الأخرى "تحلق" من خلال العمود (الصورة ب). يتبع الشطف الانتقائي سلسلة من خطوات الغسيل ثم يطلق الجزيء المستهدف (الصورة ج).
- يفصل كروماتوغرافيا التبادل الأيوني (IEX) ويركز المنتج محل الاهتمام (البروتينات ، قليل النوكليوتيدات ، وغيرها) عن المواد الأخرى القابلة للذوبان عن طريق ربط الجزيء المستهدف أو الاحتفاظ به بشكل عكسي بالعمود بناء على قوة التفاعل الكهروستاتيكي مع مادة الطور الصلب (الشكل 2 د) بينما المكونات الأخرى "تحلق" من خلال العمود. يتم استخدام IEX بانتظام كطريقة تنقية إضافية أو بديلة ، وبالتالي ، لا يقتصر على تطبيقات الالتقاط.
تعد سرعة أخذ العينات وحد الكشف (LoD) باستخدام مطياف FTIR في الموقع مثل ReactIR™ مفيدة لكروماتوغرافيا الالتقاط الأولية ، حيث تسجل نقاط قياس متعددة داخل قمم أو كسور سريعة المسح مع التفريق الكمي بين مكونات متعددة. يتيح التحليل الطيفي FTIR المضمن للمستخدمين مراقبة مدخلات التغذية المتغيرة ، بالإضافة إلى جودة الراتنج والأداء مدى الحياة ، وتحديد المكونات وتوضيحها ببصمات الأصابع ، والقضاء على التأخير في تلقي النتائج التحليلية لاتخاذ قرارات تعتمد على البيانات في الوقت الفعلي.

3. تبادل العازلة والتركيز العالي
يستخدم الترشيح الفائق (UF) بشكل متكرر في المعالجة الحيوية النهائية لتركيز تيار المنتج المخفف. يفصل الترشيح الفائق الجزيئات داخل محلول بناء على حجم مسام الغشاء أو قطع الوزن الجزيئي. غالبا ما يستخدم الترشيح الدهني (DF) لتبادل المنتج في مخزن مؤقت مطلوب (على سبيل المثال من مخزن مؤقت للشطف إلى مخزن مؤقت للتركيبة النهائية).
عادة ما يستخدم الترشيح الفائق والترشيح (المعروف معا باسم التبادل العازل) ترشيح التدفق المماسي (TFF) ، حيث يتدفق التغذية بالتوازي مع سطح الغشاء بدلا من العمودي على السطح (الشكل 3). يظل التبادل المؤقت عملية يدوية للغاية ونادرا ما يتم تحسينها. يتم تحليل تركيز المنتج بشكل عام من خلال شكل من أشكال التحليل الطيفي للأشعة فوق البنفسجية ، إما بشكل مستقل ، ككاشف ل HPLC ، أو كطريقة طول مسار متغير.
تنشأ العديد من التحديات في عملية التبادل العازل:
- تتبع دقيق لأحجام الصرف
- التنبؤ بالعملية الواثق من عينات الاستيلاء غير التمثيلية
- أوقات الاستجابة المتأخرة أو المرتفعة للقياسات غير المتصلة بالإنترنت
- الخسارة التراكمية للمنتج مع أخذ العينات الاستخراجية
- انتشار الأخطاء في تحضير العينة لقياسات الأشعة فوق البنفسجية وHPLC غير المتصلة بالإنترنت
يتيح التحليل الطيفي للأشعة تحت الحمراء ورامان في الموقع تحليل مكونات متعددة في وقت واحد ، بدقة أكبر ونطاق ديناميكي أكبر ، ودون التأخير المرتبط بالتحليل دون اتصال بالإنترنت. يمكن أن يوفر التحليل الطيفي FTIR في الموقع باستخدام ReactIR العديد من الفوائد أثناء التبادل المؤقت:
- تحديد أنواع السواغات والمواد الدوائية المتعددة في وقت واحد في الوقت الفعلي
- التحكم في استخدام المخزن المؤقت
- مراقبة تأثيرات الغشاء
- استخدم التركيز المباشر في الموقع بدلا من التقريب لحجم قطر
- زيادة دقة التركيز من +/-5٪ إلى +/- 2٪
- القضاء على التأخيرات التحليلية
تعمل المفاعلات الآلية مثل EasyMax™ على تسريع تطوير العملية بنسبة تصل إلى 80٪ من خلال التقاط البيانات التجريبية ، والتحكم الدقيق في جميع معلمات العملية الحرجة (CPPs) ، وتكامل أجهزة الاستشعار الفيزيائية الحيوية بما في ذلك الأس الهيدروجيني ، والتوصيلية الكهربية ، والأكسدة والاختزال ، والأكسجين المذاب (DO).

4. التنقية (وإزالة الملوثات أو الشوائب)
هناك العديد من الطرق المستخدمة في التسلسل والتي تستخدم لزيادة نقاء مادة الدواء (DS). بدءا من خطوات التوضيح والاستخراج المبكرة ، تليها طريقة مناسبة للالتقاط والعزل السائب الأول ، تليها لاحقا مراحل وسيطة ثم نهائية من التنقية ، وتشمل الأخيرة تلميع الكروماتوغرافيا ، والترشيح النانوي / المعقم ، والتبلور ، وإزالة الفيروس (الشكل 4).
من خلال القضاء على التأخيرات المرتبطة بالتحليل دون اتصال بالإنترنت ، تعمل قياسات FTIR في الموقع على تحسين خطوات كروماتوغرافيا التلميع من خلال توفير ملاحظات فورية لتحديد وتحديد مكونات الكسور بما في ذلك المخازن المؤقتة والمواد الدوائية والشوائب أثناء خطوات التنقية الوسيطة. ينتج عن هذا تحسين تخفيضات الكسور ، والتمييز الكلي أو الجزئي ، والتركيز الكلي في الوقت الفعلي.
للتخلص من الفيروس ، يتلف أي فيروس موجود داخل المعلق العلاجي المجمع وشبه المنقى عمدا أو يتشوه فجأة في شكل غير ممرض ، عادة عن طريق تغيير البيئة المحيطة بالفيروس. يتم تمكين التحكم في معلمات العملية الحرجة هذه (CPP) وتنقيحها من خلال منصات المفاعلات الآلية المزودة بأجهزة استشعار فيزيائية حيوية متكاملة. تعد التكنولوجيا التحليلية للعملية المضمنة (PAT) مفيدة لتوصيف الشوائب في المراحل اللاحقة من التنقية نظرا لأن التركيزات تكون أعلى بشكل عام ومن الأسهل تمييز المنتجات في مصفوفة شبه نقية.
5. الاقتران الحيوي (يعتمد على الجزيء)
تم تصميم جزيئات الاقتران الحيوي ليكون لها فعالية متزايدة ممكنة من خلال الوظيفة المشتركة لنوعين أو أكثر من أنواع الجزيئات العلاجية المختلفة. تتطلب كيمياء الاقتران الحيوي توصيفا تفصيليا للعملية وتحسينها. لم تعد الأدوات التقليدية مثل أنابيب الطرد المركزي الدقيق والأكواب والألواح الساخنة وقضبان التحريك المغناطيسية وماصات النقل قادرة على تلبية متطلبات التكرار حول الأس الهيدروجيني ودرجة الحرارة والجرعات والخلط والمعلمات الأخرى.
تعتمد كيمياء الاقتران الحيوي على سلسلة من الخطوات التي يتم التحكم فيها جيدا بالتسلسل والتي قد تشمل تقليل المجموعة الوظيفية ، والتنشيط ، واقتران رابط API مع البيولوجيا الأولية ، وأي عدد من خطوات الغسيل أو المذيبات أو التبادل المؤقت طوال الوقت (الشكل 5). يتبنى علماء المستحضرات الصيدلانية الحيوية التكنولوجيا المستخدمة بالفعل على نطاق واسع في البحث والتطوير للجزيئات الصغيرة ، مثل مفاعلات التخليق الآلي EasyMax. يوفر EasyMax بنية متماسكة بحيث يتم التحكم بدقة في معلمات العملية ذات الصلة بما في ذلك الأس الهيدروجيني ، والتوصيلية الكهربية ، والأكسدة والاختزال ، ودرجة الحرارة ، والتحريك ، والجرعات ، وما إلى ذلك ، ويتم التقاط البيانات التجريبية بدقة. توفر أتمتة كيمياء الاقتران الحيوي تكامل البيانات ، وارتباط أحداث العملية ، والسلامة التجريبية ، ومعلمات توسيع نطاق تصميم التجربة (DoE ).
يتيح EasyMax التقييم السريع والتحكم الدقيق في CPP لمساحة دائرة الطاقة، بما في ذلك ظروف الخلط والتحكم في درجة الحرارة واستراتيجيات الجرعات والمعدلات. القضاء على التباين التجريبي المرتبط بالطرق اليدوية غير المتصلة بالإنترنت وضعف عناصر التحكم في معلمات العملية الحرجة. يمكن أن يوفر التحليل الطيفي FTIR و Raman في الموقع معلومات ميكانيكية مفصلة في الوقت الفعلي ، مما يلغي التأخيرات دون اتصال بالإنترنت وعدم دقة أخذ العينات.


6. الصياغة
الهدف من الصياغة هو نقل جزيء المنتج من بيئة أو مذيب أو حالة فيزيائية أخرى تستخدم لتصنيع المنتج إلى شكل مقبول للإدارة السريرية البشرية (الشكل 6). تمت صياغة جزيء المنتج وفقا لكيفية استخدام المنتج النهائي عن طريق الاستنشاق أو الحقن أو الجرعات عن طريق الفم. يتم تقييم الاستقرار طويل الأجل للمنتج والسواغات المرتبطة به للتأكد من أن الجرعة المقاسة وسمات الجودة الحرجة (CQAs) ضمن المواصفات بعد المعالجة والتخزين والشحن. إلى جانب العقم ، يعد ضمان إزالة الشوائب والسموم الداخلية ومنع تدهور منتج الدواء (DP) أمرا ضروريا للحفاظ على السلامة والفعالية أثناء تصنيع وتخزين البروتين العلاجي على المدى الطويل.
تشمل المنتجات الدوائية المركبة البروتينات (على وجه التحديد mAb) ، والسكريات ، وأنظمة الجسيمات النانوية ، والمواد العضوية ، وقليل النوكليوتيدات ، والعلاجات الجينية ، والعديد من أنواع اللقاحات. سيتم صياغة بعض اللقاحات بمادة مساعدة ، عادة ما تكون عبارة عن جسيمات أساسها الألومنيوم أو مستحلب عضوي. تعد صياغة اللقاح والتخليق المساعد ، على وجه الخصوص ، تدفقات عمل في وضع جيد للاستفادة من محطات عمل المفاعلات المتوازية الآلية ، ورقمنة سير العمل ، والتكنولوجيا التحليلية للعمليات المتعامدة (PAT) تكامل. باستخدام PAT في الوقت الفعلي ، يتم الحصول على المزيد من المعرفة حول العملية ، بدلا من تحليل البداية ونقاط النهاية فقط.
تتحكم أنظمة المفاعلات المتوازية مثل EasyMax في جميع معلمات العملية الهامة وتدمج أدوات PAT المضمنة مثل ReactIR و ReactRaman™ و ParticleTrack و EasyViewer ، من بين أجهزة الاستشعار الفيزيائية الحيوية الأخرى. كثيرا ما تستخدم هذه التقنيات في الصياغة لتوصيف استقرار مادة الدواء والمنتج الدوائي ، والتركيز النهائي ، والتخليق المساعد ، والبلمرة ، والتغليف ، والامتصاص ، وأحداث الجسيمات الأخرى.
موارد إضافية
منتجات ذات صله
الاستشهادات والمراجع
منشور مميز: ترسيب كلوريد الزنك لالتقاط الأجسام المضادة المؤتلفة
يدعم EasyMax و ParticleTrack تنقية
دوترا ، جي ، كوموتشيكي ، د. ، جونغباور ، أ. ، واتسر ، ب. (2020). الالتقاط المستمر للأجسام المضادة المؤتلفة بواسطة ZnCl2 ترسيب بدون البولي إيثيلين جلايكول. الهندسة في علوم الحياة ، 20 (7) ، 265-274. https://doi.org/10.1002/elsc.201900160
أفاد المؤلفون باستخدام الكاتيونات ثنائية النسيلة ، وتحديدا ZnCl2 ، لالتقاط وتنقية الأجسام المضادة وحيدة النسيلة بطريقة قائمة على ترسيب الأمطار. بسبب طبيعة التشابك للكاتيونات ثنائية النسيلة والقضاء على PEG ، كانت اللزوجة من عوامل التخفيف الطافية والقابلة للذوبان منخفضة للغاية.
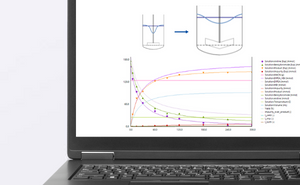
من خلال الحفاظ على تركيز ZnCl2 ثابتا وتغيير الأس الهيدروجيني باستخدام مفاعل مختبر آلي EasyMax ، حدد المؤلفون تأثير الأس الهيدروجيني على الغلة. تمت مراقبة هطول الأمطار باستخدام مسبار ParticleTrack FBRM وتم قياس توزيع حجم مجموعات البروتين عند درجة الحموضة المختلفة. ووجدوا أن الرقم الهيدروجيني الأمثل لهطول الأمطار يبلغ حوالي الرقم الهيدروجيني 6 و 7 ، وأن الأس الهيدروجيني له تأثير كبير على حجم مجموعات الترسيب ، مع وجود أكبر مجموعات مرتبطة بعوائد أفضل. ويذكرون أنه يمكن استخدام المراقبة المضمنة ل FBRM لتقدير الإنتاجية الناتجة دون قياس التركيز الفعلي أثناء هطول الأمطار.

منشور مميز: التحقيق الفيزيائي والكيميائي لمساعد فوسفات الألومنيوم
تدمج منصة EasyMax التحليل الطيفي في الموقع وتوصيف الجسيمات
مي ، سي ، ديشموخ ، إس إس ، كرونين ، جي تي ، كونغ ، إس ، تشابمان ، دي بي ، لازاريس ، إن ، سامباليانو ، إل ، شاخت ، يو ، دروليت فيفز ، ك. ، أور ، إم أو ، مورين ، إس ، كاربيك ، ب. ، بالمر ، إم تي ، وكيركيتادزه ، م. (2019). مساعد لقاح فوسفات الألومنيوم: تحليل التركيب والحجم باستخدام أدوات غير متصلة ومدمجة. مجلة التكنولوجيا الحيوية الحسابية والهيكلية ، 17, 1184-1194. https://doi.org/10.1016/j.csbj.2019.08.003
نظرا لأن التفاعل بين المستضد والمساعد مهم لمناعة اللقاح ، فقد قام المؤلفون بالتحقيق في الخصائص الفيزيائية والكيميائية للمادة المساعدة ، في هذه الحالة AlPO4 ، مثل حجم الجسيمات والتركيب الكيميائي. استخدموا كلا من التقنيات غير المتصلة بالإنترنت مثل الأشعة تحت الحمراء لتحويل فورييه (FTIR)والتحليل الطيفي رامان ، والتحليل الطيفي للإلكترون الضوئي بالأشعة السينية (XPS) ، وحيود الليزر ، والطرق المضمنة بما في ذلك التحليل الطيفي ATR-FTIR في الموقع (ReactIR) ، وتحليل طيفي رامان (ReactRaman) ، وقياس انعكاس الحزمة المركزة (FBRM ، ParticleTrack). فيما يتعلق بالقياسات المضمنة ، تم فحص توزيع حجم الجسيمات لفوسفات الألومنيوم والبروتين الممتز بواسطة FBRM ، وتم إجراء التحليل التركيبي لفوسفات الألومنيوم باستخدام مسبار ATR في الموقع.
وخلص المؤلفون إلى أن PAT المضمنة تراقب بشكل فعال حجم الجسيمات والتركيب الكيميائي للمراحل المختلفة من التصنيع المساعد. يمكن استخدام أساليب مماثلة للمساعدة في تقييم الاتساق من الكثير إلى الدفعة أيضا. يذكرون أن استخدام PAT المضمن يدعم استراتيجيات التصنيع المتقدمة مثل اختبار إصدار المنتج في الوقت الفعلي.
المعالجة النهائية في المنشورات التي يراجعها الأقران
فيما يلي مجموعة مختارة من المنشورات الحديثة حول المعالجة النهائية في التكنولوجيا الحيوية وصناعة المستحضرات الصيدلانية الحيوية.
- جارج ، إم ، وراثور ، إيه إس (2023). تطبيق PAT في تصنيع الأدوية: التحكم القائم على النموذج في توزيع حجم الجسيمات في التبلور بمساعدة المذيبات. مجلة التكنولوجيا الكيميائية والتكنولوجيا الحيوية ، 98 (12) ، 2806-2811. https://doi.org/10.1002/jctb.7497
- دوترا ، جي ، كوموتشيكي ، د. ، جونغباور ، أ. ، واتسر ، ب. (2020). التقاط مستمر للأجسام المضادة المؤتلفة بواسطة ZnCl2 الترسيب بدون البولي إيثيلين جلايكول. الهندسة في علوم الحياة ، 20 (7) ، 265-274. https://doi.org/10.1002/elsc.201900160
- Wasalathanthri ، D. P. ، Rehmann ، M. S. ، Song ، Y. ، Gu ، Y. ، Luo ، M. ، Shao ، C. ، Chemmalil ، L. ، Lee ، J. ، Ghose ، S. ، Borys ، M. ، Ding ، J. ، Li ، Z. J. (2020). التوقعات التكنولوجية لمراقبة سمة الجودة ومعلمات العملية في الوقت الفعلي في تطوير المستحضرات الصيدلانية الحيوية - مراجعة. التكنولوجيا الحيوية والهندسة الحيوية ، 117 (10) ، 3182-3198. https://doi.org/10.1002/bit.27461
- مي ، سي ، ديشموخ ، إس إس ، كرونين ، جي تي ، كونغ ، إس ، تشابمان ، دي بي ، لازاريس ، إن ، سامباليانو ، إل ، شاخت ، يو ، دروليت فيفز ، ك. ، أور ، إم أو ، مورين ، إس ، كاربيك ، ب. ، بالمر ، إم تي ، وكيركيتادزه ، م. (2019). مساعد لقاح فوسفات الألومنيوم: تحليل التركيب والحجم باستخدام أدوات Off-Line و In-Line. مجلة التكنولوجيا الحيوية الحاسوبية والهيكلية ، 17, 1184–1194. https://doi.org/10.1016/j.csbj.2019.08.003
- Kager ، J. ، Berezhinskiy ، V. ، Zimmerleiter ، R. ، Brandstetter ، M. ، & Herwig ، C. (2019). تمديد مرشح الجسيمات لتقدير حالة العملية الحيوية باستخدام قياسات الأشعة تحت الحمراء الغازية وغير الغازية. في الهندسة الكيميائية بمساعدة الكمبيوتر (ص 1417-1422). https://doi.org/10.1016/b978-0-12-818634-3.50237-x
- برونر ، إم ، بروسيج ، ب. ، لوسينج ، إم ، كونزلمان ، إم ، كالفيت ، إيه ، ستيفل ، إف ، بيكشمان ، جيه ، أونسويلد ، أ. ، وشوب ، ج. (2019). نحو عمليات زراعة الخلايا القوية - كشف تأثير إعداد الوسائط عن طريق المراقبة الطيفية عبر الإنترنت. الهندسة في علوم الحياة ، 19 (10) ، 666-680. https://doi.org/10.1002/elsc.201900050
- Deshors، M.، Guais، O.، Neugnot-Roux، V.، Cameleyre، X.، Fillaudeau، L.، & François، J. (2019). الجمع بين الأساليب الكيميائية الحيوية الفيزيائية وخارج الموقع في الموقع للتحقيق في التفكيك في المختبر لنخالة القمح المنزوعة النشا بواسطة كوكتيل الإنزيمات المستخدمة في تغذية. الحدود في الهندسة الحيوية والتكنولوجيا الحيوية ، 7. https://doi.org/10.3389/fbioe.2019.00158
- Großhans، S.، Rüdt، M.، Sanden، A.، Brestrich، N.، Morgenstern، J.، Heißler، S.، & Hubbuch، J. (2018). التحليل الطيفي بالأشعة تحت الحمراء لتحويل فورييه كتقنية تحليلية متعددة الاستخدامات لكروماتوغرافيا البروتين التحضيرية. مجلة الكروماتوغرافيا أ ، 1547 ، 37-44. https://doi.org/10.1016/j.chroma.2018.03.005
- ليموين ، أ. ، ديلفين ، ف. ، بوكيش ، أ. ، نيوباور ، ب. ، وجون ، س. (2017). أدوات لتحديد عدم التجانس السكاني الناجم عن ظروف الزراعة غير المتجانسة. مجلة التكنولوجيا الحيوية ، 251, 84–93. https://doi.org/10.1016/j.jbiotec.2017.03.020
- ديركسن ، أ. ، ديفيس ، ك. أ. ، كولينز ، جيه ، بهاتاشاريا ، ك. ، فينيمان ، جي آي ، بيبين ، إي إل ، ريكزيك ، جي إس ، براون ، بي ، ويلبورن ، دبليو بي ، مانجالاتهيلام ، ر. ، إيفانز ، ب. ، بوزو ، إم جيه ، فين ، آر إف (2017). تطوير عملية اقتران البروتين والأجسام المضادة FGF21. علم الببتيد ، 110 (1). https://doi.org/10.1002/bip.23042
- كوخ ، سي ، بوش ، إيه إي ، هيرويج ، سي ، وليندل ، ب. (2016). مقارنة بين الألياف البصرية والقناة الانعكاس الكلي الموهن (ATR) فورييه تحويل الأشعة تحت الحمراء (FT-IR) إعداد لمراقبة التخمير في الخط. التحليل الطيفي التطبيقي ، 70 (12) ، 1965-1973. https://doi.org/10.1177/0003702816662618
- سالازار ، أ. ، بليفوس ، ج. ، سيمون ، أ. ، شوسلر ، إس ، كيوسجن ، إم ، ستانكيفيتش ، إن آر ، وفون هاغن ، ج. (2016). يؤدي ضغط وسائط زراعة الخلايا المحددة كيميائيا إلى زيادة معدل الذوبان من خلال زيادة مساحة السطح التي يمكن الوصول إليها بواسطة المذيبات. تكنولوجيا المسحوق ، 301 ، 110-117. https://doi.org/10.1016/j.powtec.2016.05.065
- لوبيز إكسبوزيتو ، ب. ، سواريز ، أ. ب. ، ونيغرو ، سي (2015). تقدير تركيز الكتلة الحيوية Chlamydomonas reinhardtii من بيانات توزيع طول الوتر. مجلة علم الفيكوولوجيا التطبيقي, 28(4), 2315–2322. https://doi.org/10.1007/s10811-015-0749-4
- سيبليست ، سي ، جينزش ، إم ، وبولشيدت ، م. (2015). توصيف المعدات للتخفيف من المخاطر أثناء عمليات تصنيع زراعة الخلايا. تكنولوجيا الخلايا ، 68 (4) ، 1381-1401. https://doi.org/10.1007/s10616-015-9899-0
- فاجاتشيفسكي ، ج. ، سيلين ، د. ، فيدنهوفر ، سي ، بوهني ، إس ، تريو ، إتش كيه ، هيلترهاوس ، ل. (2015). تم حله مكانيا في الموقع لتحديد تقدم التفاعل باستخدام أنظمة الموائع الدقيقة والتحليل الطيفي FT-IR كأداة لتطوير عملية التحفيز الحيوي. هندسة العمليات الحيوية والنظم الحيوية ، 38 (7) ، 1399-1405. https://doi.org/10.1007/s00449-015-1381-z
- وو ، إتش ، ريد ، إي كي ، وايت ، إم ، شافيز ، ب. ، برورسون ، ك. ، أغاربي ، سي ، وخان ، إم إيه (2015). المراقبة في الوقت الفعلي لديناميكيات عملية زراعة الخلايا للمفاعل الحيوي mAb IgG3 عبر التحليل الطيفي بالأشعة تحت الحمراء لتحويل فورييه: الآثار المترتبة على تمكين التكنولوجيا التحليلية لعملية زراعة الخلايا. حدود العلوم الكيميائية والهندسة ، 9 (3) ، 386-406. https://doi.org/10.1007/s11705-015-1533-3
- كوخ ، سي ، بوش ، إيه إي ، جويكوتشيا ، إتش سي ، هيرويج ، سي ، وليندل ، ب. (2014). القياس الكمي متعدد التحليلات في العمليات الحيوية عن طريق التحليل الطيفي بالأشعة تحت الحمراء بتحويل فورييه عن طريق انحدار المربعات الصغرى الجزئية ودقة المنحنى متعددة المتغيرات. أناليتيكا شيميكا أكتا ، 807 ، 103-110. https://doi.org/10.1016/j.aca.2013.10.042
- والثر ، سي ، ماير ، س. ، جونغباور ، أ. ، ودوراور ، أ. (2014). الاستعداد ل PAT: توسيع نطاق ومراقبة إعادة طي البروتين لبروتينات اندماج Npro. عملية الكيمياء الحيوية ، 49 (7) ، 1113-1121. https://doi.org/10.1016/j.procbio.2014.03.022
- Tscheließnig ، A. ، Satzer ، P. ، Hammerschmidt ، N. ، Schulz ، H. ، Helk ، B. ، & Jungbauer ، A. (2014). ترسيب الإيثانول لتنقية الأجسام المضادة المؤتلفة. مجلة التكنولوجيا الحيوية ، 188, 17–28. https://doi.org/10.1016/j.jbiotec.2014.07.436
- Sagmeister ، P. ، Kment ، M. ، Wechselberger ، P. ، Meitz ، A. ، Langemann ، T. ، & Herwig ، C. (2013). التحقيق الديناميكي بمساعدة المستشعر الناعم للعمليات الحيوية للأعلاف المختلطة. عملية الكيمياء الحيوية ، 48 (12) ، 1839-1847. https://doi.org/10.1016/j.procbio.2013.09.018
- Sagmeister ، P. ، Langemann ، T. ، Wechselberger ، P. ، Meitz ، A. ، & Herwig ، C. (2013). طريقة ديناميكية للتحقيق في قدرات التمثيل الغذائي للحالة المستحثة كدالة لدرجة الحرارة. مصانع الخلايا الميكروبية ، 12 (1). https://doi.org/10.1186/1475-2859-12-94
- دالباكا ، ج. ، كيفيهارجو ، ك. ، إيريكينين ، ت. ، وفاجيرفيك ، ك. (2012). رصد زراعة Streptomyces peucetius باستخدام التحليل الطيفي FTIR / ATR والنماذج الكمية بناء على بيانات نوع المكتبة. رسائل التكنولوجيا الحيوية ، 35 (3) ، 337-343. https://doi.org/10.1007/s10529-012-1093-2
- دالباكا ، ج. ، ويغار ، ج. ، فون ويمارن ، ن. ، وفاجرفيك ، ك. (2012). القياس عبر الإنترنت لتركيزات الركيزة في تخمير Pichia pastoris باستخدام FT-IR / ATR. رسائل التكنولوجيا الحيوية ، 34 (6) ، 1009-1017. https://doi.org/10.1007/s10529-012-0868-9
- Landgrebe ، D. ، Haake ، C. ، Höpfner ، T. ، Beutel ، S. ، Hitzmann ، B. ، Scheper ، T. ، Rhiel ، M. ، & Reardon ، K. F. (2010). التحليل الطيفي بالأشعة تحت الحمراء عبر الإنترنت لمراقبة العمليات الحيوية. علم الأحياء الدقيقة التطبيقي والتكنولوجيا الحيوية ، 88 (1) ، 11-22. https://doi.org/10.1007/s00253-010-2743-8
- دابروس ، إم ، شولر ، إم إم ، وماريسون ، آي دبليو (2010). تحكم بسيط في معدل النمو المحدد في عمليات الدفعات الفيدرالية في التكنولوجيا الحيوية بناء على قياسات محسنة عبر الإنترنت للكتلة الحيوية. هندسة العمليات الحيوية والنظم الحيوية ، 33 (9) ، 1109-1118. https://doi.org/10.1007/s00449-010-0438-2
- مولر ، ج. ، نيومان ، إم ، شول ، ب. ، هيلترهاوس ، إل ، إيكشتاين ، إم ، ثوم ، أو ، ولي ، أ. (2010). المراقبة عبر الإنترنت للتحولات الحيوية في الأنظمة متعددة المراحل عالية اللزوجة عن طريق FT-IR والقياسات الكيميائية. الكيمياء التحليلية ، 82 (14) ، 6008-6014. https://doi.org/10.1021/ac100469t