Йетра, С. Р., Шмитт, Н., и Тамбар, У. К. (2022). Каталитическое фотохимическое энантиоселективное α-алкилирование солями пиридиния. Химическая наука, 14 (3), 586–592. https://doi.org/10.1039/d2sc05654b
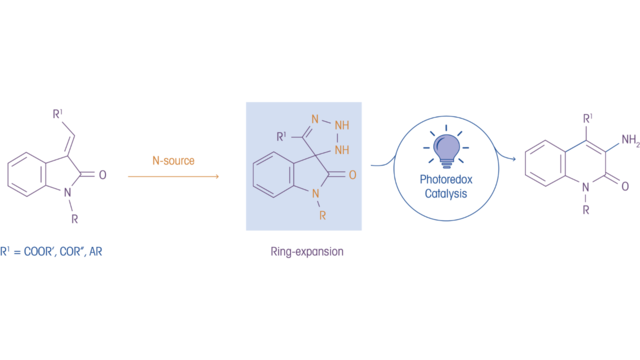
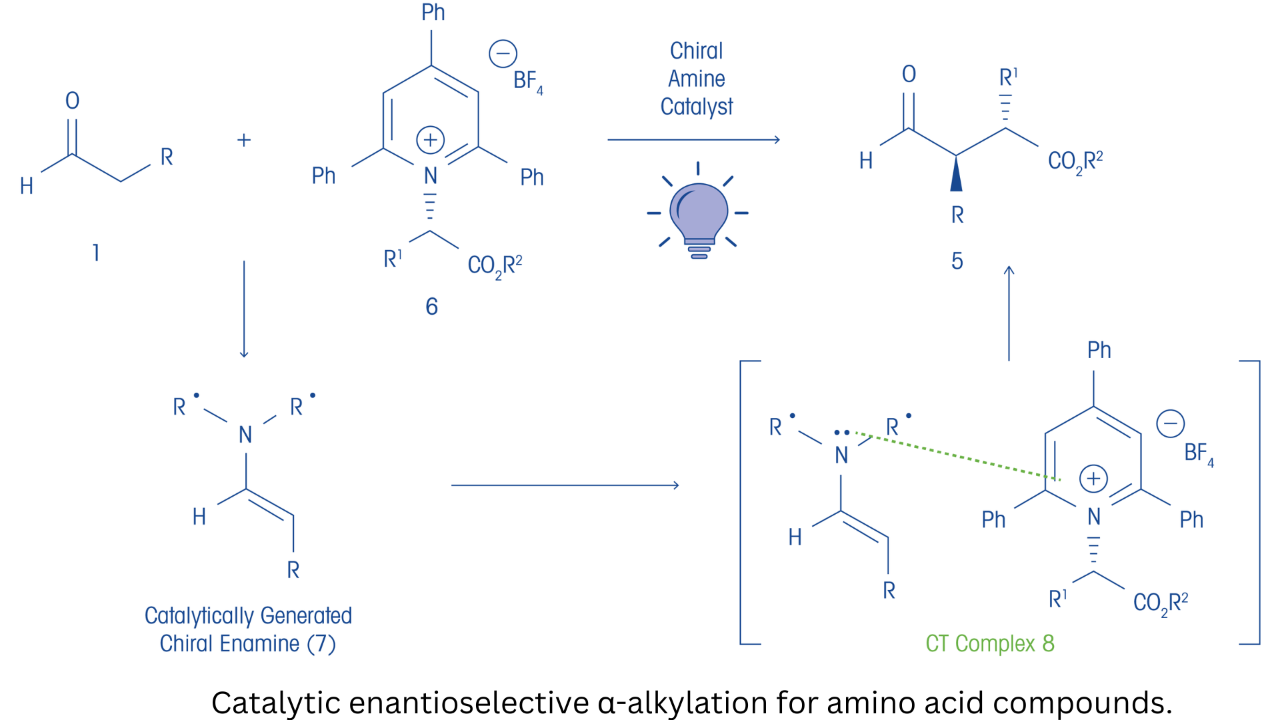
Авторы отметили, что алкилгалогениды и сульфонаты часто используются в алкилирующих агентах, используемых в асимметричном катализе для энантиоселективного α-алкилирования енолатов. Их интерес заключался в разработке фотохимического процесса энантиоселективного алкилирования, в котором используются возобновляемые и устойчивые источники алкилирующих реагентов, такие как субстраты, полученные из аминокислот. Учитывая низкую способность производных аминокислот к принятию электронов в енолированных алкилированиях, задача заключалась в том, чтобы разработать средства для активации этих соединений. Основываясь на более ранних работах в литературе, авторы предположили, что использование солей пиридиния, полученных из аминокислот, в качестве алкилирующих агентов будет эффективным, учитывая, что соли пиридиния, как известно, используются в качестве радикальных предшественников в энантиоселективных α-алкилатионах. Они предположили, что соли пиридиния образуют комплексы основного состояния с каталитически генерируемыми, богатыми электронами хиральными эквивалентами енолатов. В обширной серии экспериментов они показали, что электронно-дефицитная соль Катрицкого, полученная из 2,2,2-трифторэтилового эфира глицина, прореагировавшая в условиях с использованием хирального аминового катализатора, 2,6-лютидина и облучения 427 нм, обеспечивает желаемый продукт α-алкилирования.
Дополнительная работа показала, что использование основной среды Льюиса, такой как диметилацетамид, улучшило выход продукции (до 40%) и обеспечило превосходный энантиомерный избыток (т.е. 92%). Кроме того, использование добавок, таких как йодид натрия, которые улучшают комплексообразование компонентов реакции в основном состоянии, привело к получению 75% при 92% ee. В ходе углубленных механистических исследований они предположили, что каталитическая энантиоселективная реакция может протекать одновременно через механизм радикальной комбинации в клетке и механизм радикальной цепи. Исследователи продолжили изучение сферы фотокаталитической реакции, в том числе с использованием этого процесса в общем синтезе природных продуктов лигнана (-)-энтеролактона и (-)-энтеродиола.
Ключевым наблюдением в их работе была критическая важность контроля температуры реакции. Проведение этих реакций при комнатной температуре отрицательно влияло на энантиоселективность, а поддержание 92% ee требовало запуска реакции при температуре 4 °C. Контроль температуры был сложной задачей, так как реакция постоянно облучалась источником света рядом с сосудом. По этой причине исследователи использовали систему EasyMax 102. В статье, посвященной работе профессора Тамбура по каталитическому фотохимическому энантиоселективному α-алкилированию с использованием солей пиридиния (Synform, 2023/06, A100-A105), он комментирует: «Мы наконец-то приобрели усовершенствованную термостатную систему EasyMax 102 у Mettler-Toledo AutoChem, Inc. Это оказалось самой важной покупкой для успеха проекта. Несмотря на то, что EasyMax никогда не использовался для фотохимических реакций, мы выделили две ключевые особенности этого прибора. Во-первых, это позволяет поддерживать постоянную низкую температуру реакции в течение длительного времени. Во-вторых, прибор имеет прозрачное окно в реакционную камеру, которое обычно используется для просмотра
в реакцию, но мы определили это как возможность излучать свет от лампы на контролируемом расстоянии, не влияя на температуру реакции. К нашему удовольствию, EasyMax обеспечил новый уровень стабильности в наших результатах».