Na indústria farmacêutica, o monitoramento microbiano de Água Purificada, Água Ultrapura e Água para Injeção não é apenas uma boa prática de controle de qualidade; é um requisito regulatório. Os padrões estabelecidos pela Farmacopeia dos Estados Unidos (USP) determinam as condições sob as quais a contaminação microbiana deve ser testada.
Por exemplo, a USP <61> descreve os requisitos para limites microbianos, especificando níveis aceitáveis de microrganismos em produtos não estéreis e enfatizando a importância da qualidade da água. A USP <62> detalha métodos para detectar patógenos específicos, incluindo E. coli, Salmonella e Pseudomonas aeruginosa, em água esterilizada. Além disso, a USP <1231> sobre Água para Fins Farmacêuticos da USP tem endossado consistentemente o monitoramento on-line e contínuo de águas farmacêuticas. Essa abordagem garante que os dados históricos em processo sejam coletados, permitindo o controle eficaz dos sistemas de água e mantendo a produção de água que atenda aos padrões de qualidade aceitáveis.
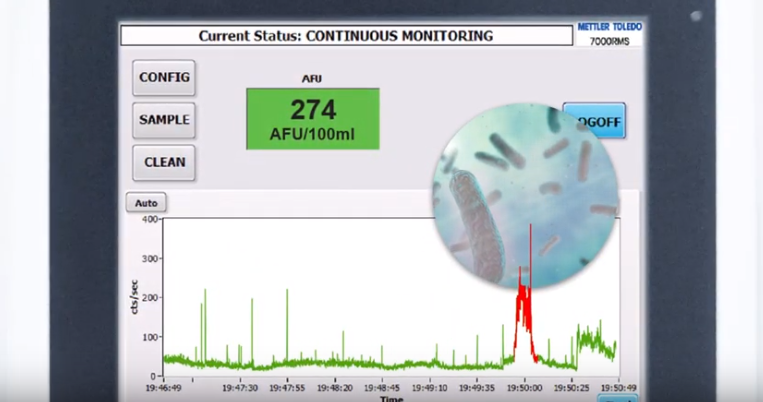
O 7000RMS está alinhado com a USP <1223>, que incentiva a validação de métodos alternativos que demonstram vantagens em precisão e sensibilidade. Ele também segue as diretrizes publicadas pela FDA e EMA para métodos alternativos de medição microbiológica, garantindo a conformidade com os padrões regulatórios e aprimorando o processo de monitoramento.


.png/_jcr_content/renditions/cq5dam.web.1280.1280.png)